

铁死亡专题(二)铁死亡与肿瘤耐药
 2021-11-09 14:31:02
2021-11-09 14:31:02
来源/作者:普拉特泽-生物医学整体课题外包平台
朋友们,大家好~在上一期内容中,我们带大家初步了解了国自然大热铁死亡的背景,想要复习的同学可以移步上一篇推文:
本期我们将通过典型文献讲解,CISD2 inhibition overcomes resistance to sulfasalazine-induced ferroptotic cell death in head and neck cancer, 带大家了解铁死亡如何与肿瘤耐药联系起来。该文献于2018年发表于老牌肿瘤学杂志cancer letters上,最新影响因子7.5。
背景知识
在讲解正文之前,我们得先了解几条背景知识。首先,在肿瘤中诱导铁死亡,能够诱导耐药的癌细胞的死亡,无论是作为单一疗法,还是与其他化疗药物或放疗联合使用。
xCT和谷胱甘肽过氧化物酶(GPX4)是铁死亡过程的关键调控分子。xCT用胞外胱氨酸交换胞内谷氨酸,作为细胞内主要抗氧化剂谷胱甘肽(GSH)的来源,xCT可抑制脂质过氧化作用,从而抑制铁死亡。
Sulfasalazine (SAS)是xCT的抑制剂,也就是一种铁死亡的诱导剂。SAS处理细胞已被证实能够有效抑制肿瘤细胞的生长,但是肿瘤细胞也会发展出对包括SAS在内的铁死亡抑制剂的耐药。
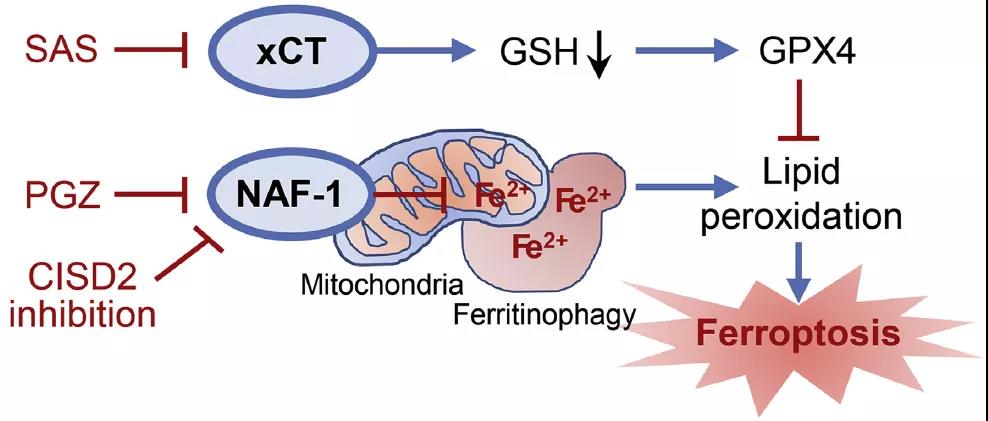
该研究研究的关键基因CISD2(基因名CISD2,编码蛋白NAF-1)的主要功能是是将2Fe-2S簇转移到apo受体蛋白上,并将铁转移到线粒体上。而该研究主要就是探索调控CISD2这一基因的表达如何使肿瘤细胞对铁死亡诱导剂SAS变得敏感。作者提供的思路图大概是这样:
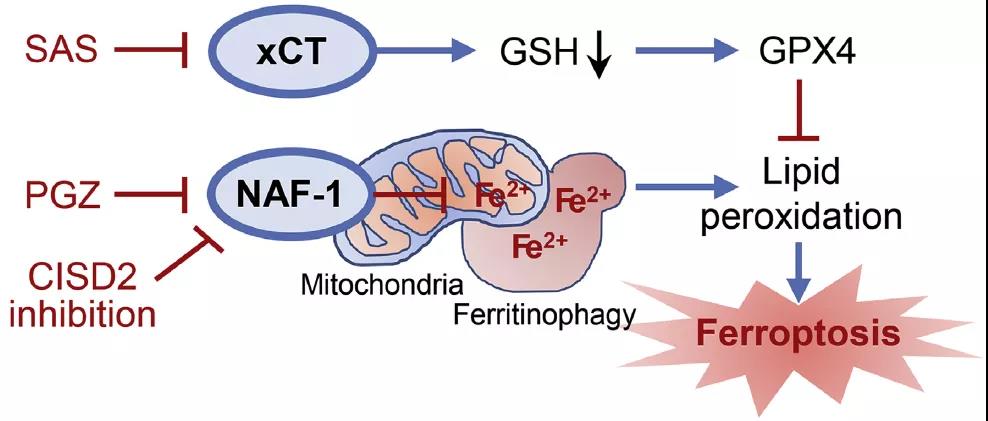
好了,介绍完背景知识,我们来看看作者是怎么做验证的(文中仅展示核心结果,完整的结果大家可以自行阅读文献进行补完)。
验证过程
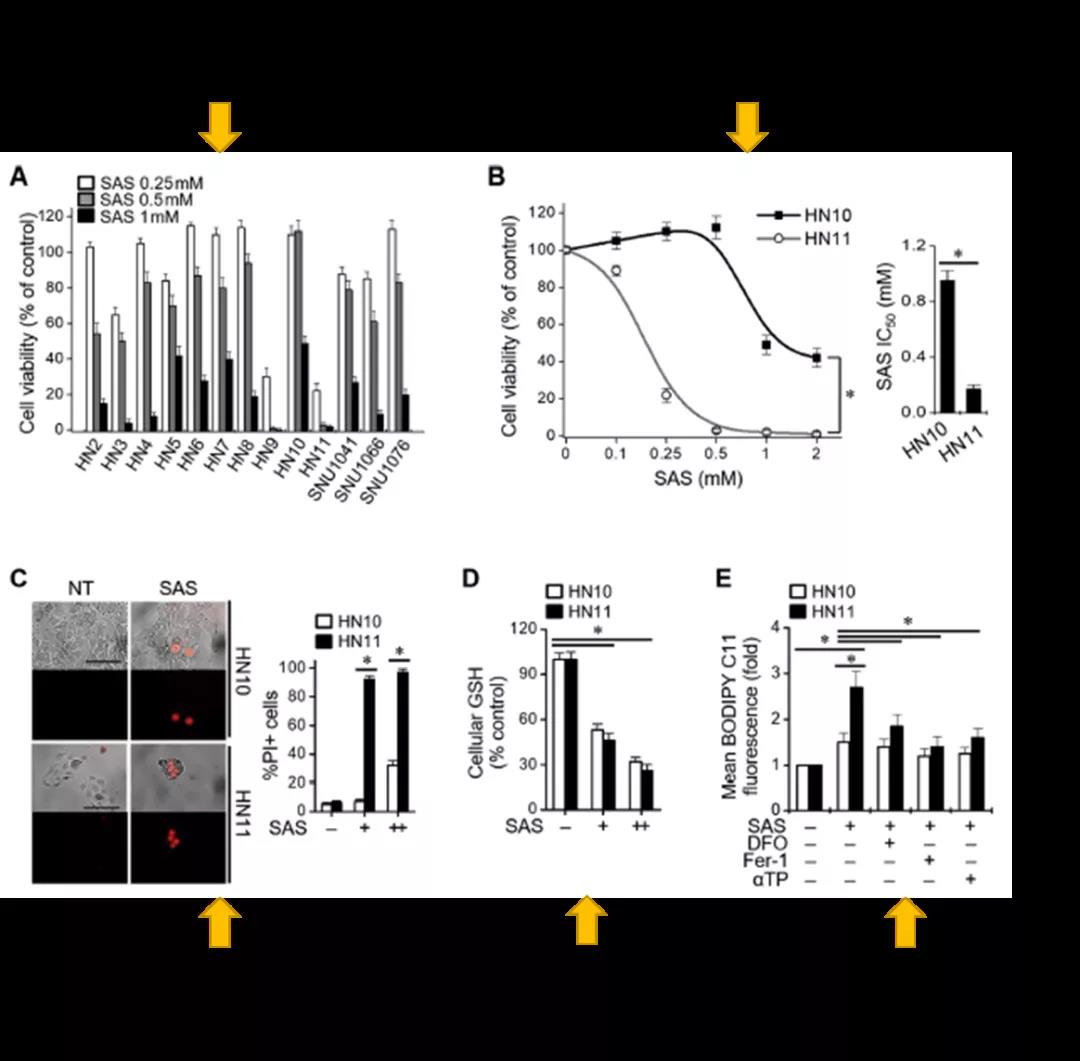
首先作者使用SAS处理头颈癌细胞系,发现各细胞系对SAS的敏感性不同。其中HN10呈现出最耐受,而HN11呈现出最敏感。通过进一步的检测发现,SAS在HN10和HN11中诱导的GSH的变化无差异,但是脂质过氧化水平HN11细胞系更高,说明SAS在两株细胞中诱导的铁死亡程度也不同。
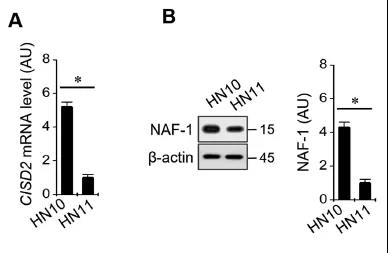
接下来,作者在HN10和HN11两株细胞中检测关键基因CISD2 (NAF-1)的表达情况,发现对SAS敏感的HN11中NAF-1的表达较不敏感的HN10要少。
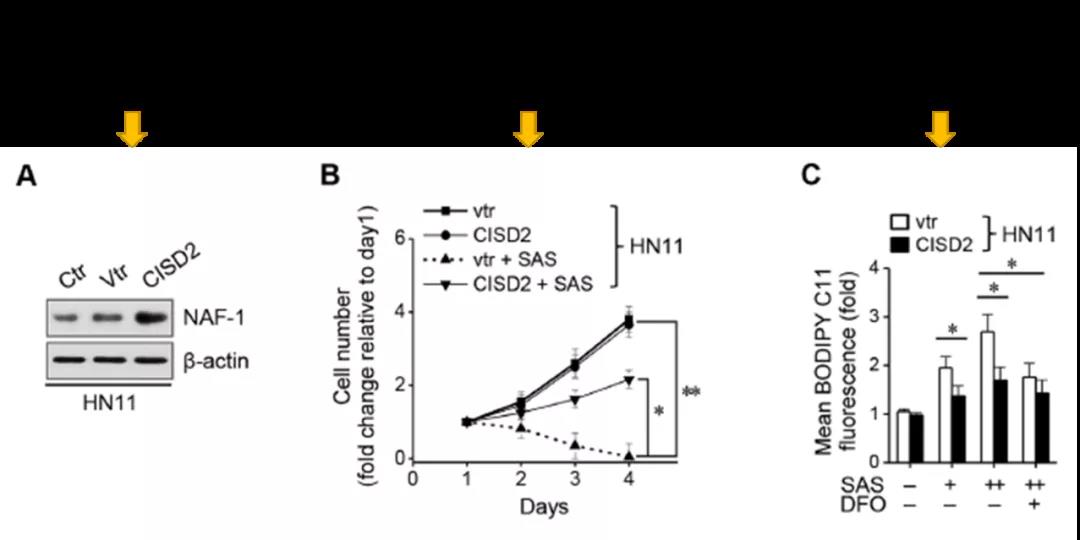
然后作者分别在表达CISD2少的HN11中过表达了CISD2, 在表达CISD2多的HN10细胞中敲降了CISD2。结果可想而知,HN11中过表达CISD2后,对SAS诱导的细胞死亡和铁死亡变得不敏感,而敲出了CISD2的HN10细胞,对SAS的敏感性显著上升。
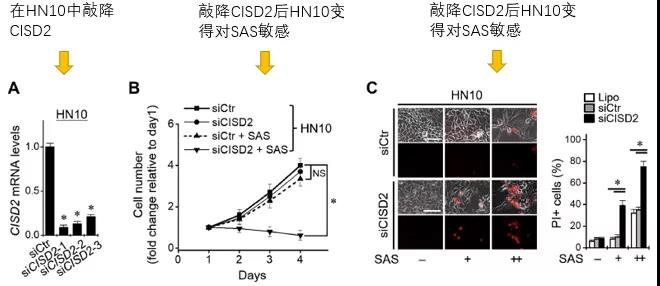
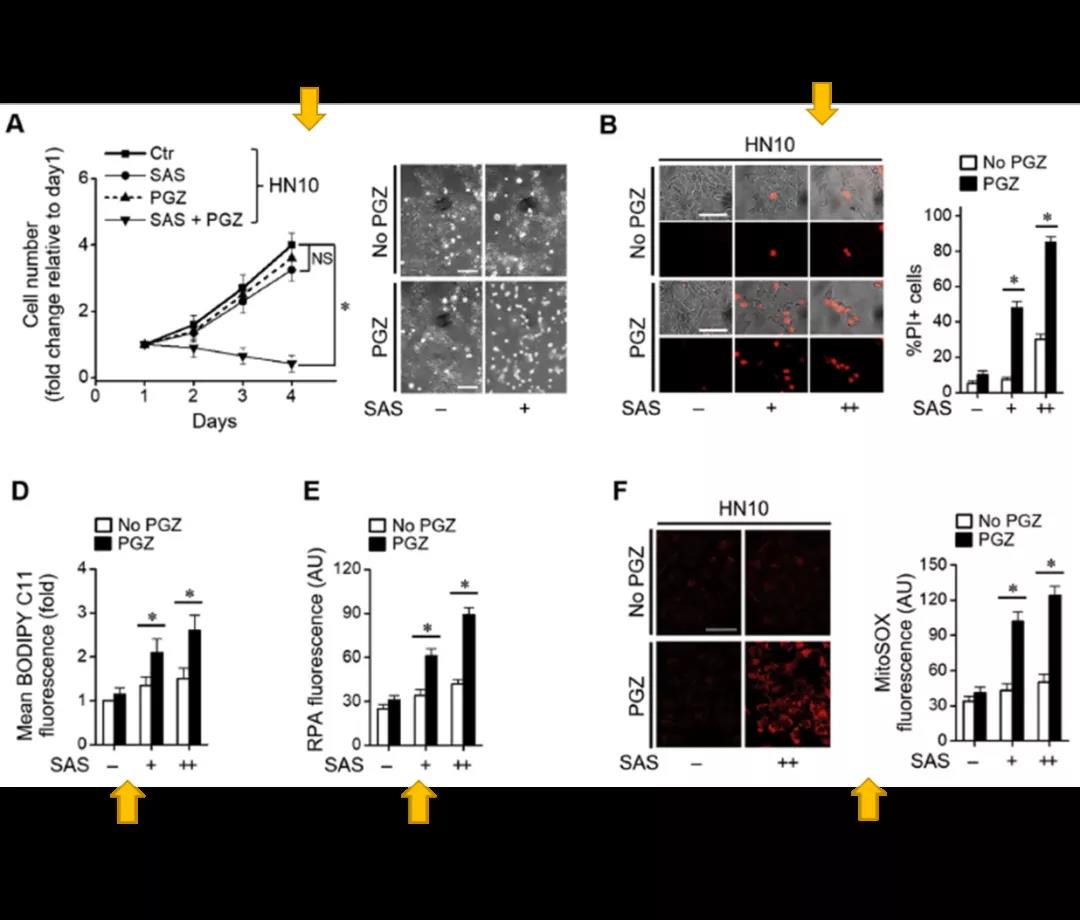
著名的降糖药Pioglitazone (PGZ)是PPARγ的激动剂,其同时也可以抑制CISD2的活性。接下来,作者通过PGZ与SAS联用的方式验证PGZ是否对SAS有增敏作用。结果显示PGZ联用能够显著升高细胞对SAS的敏感性,同时升高细胞内铁死亡的水平。
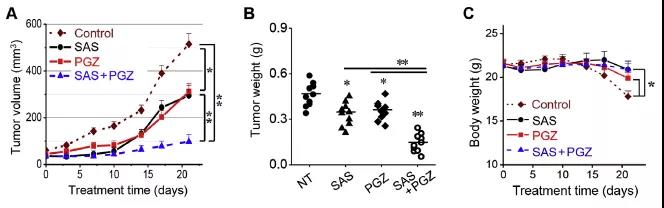
最后,通过体内成瘤实验,进一步证实了PGZ对SAS的增敏作用。
至此,作者完成了其主要论证。结合思路图我们可以发现文章的主要思路非常的简洁:通过干扰某个基因(CISD2),观察细胞对铁死亡诱导剂(SAS)的敏感性变化。简单分析一下为什么发的分数不低,当然一是关键分子选得新,二是选择了多种细胞系进行论证,三是在最后加入了药物联用,为研究应用于临床提供了前景,这些点都是我们可以借鉴的。
科研的世界千奇百怪,科研的套路千千万万,用术业专攻的内容带你解惑科研的很多问号。
