

肿瘤微环境(一)肿瘤相关巨噬细胞与血管生成
 2021-11-02 16:22:24
2021-11-02 16:22:24
来源/作者:普拉特泽生物-医学整体课题外包
肿瘤相关巨噬细胞(Tumor-associated macrophages,TAMs)是指浸润在肿瘤组织中的巨噬细胞,是肿瘤微环境(TME)的重要组成。
一般来说,这些TAM能够通过旁分泌的方式,促进肿瘤细胞的浸润和迁移。
针对TAM的研究一般聚焦于TAM分泌的X分子通过调控肿瘤细胞内的信号通路,促进肿瘤的发生发展;也有反过来研究肿瘤细胞如何诱导TAM往具有促癌作用的M2型分化的。
今天带大家了解的这篇文献可谓另辟蹊径,研究了关于TAM如何调控肿瘤微环境中的血管新生(Neovascularization),或许可以给大家在国自然的设计上带来不一样的启发。这篇文献于2017年发表在oncogene上,影响因子常年维持在6-7分的区间。
Zhu C , Chrifi I , Mustafa D , et al. CECR1-mediated cross talk between macrophages and vascular mural cells promotes neovascularization in malignant glioma[J]. Oncogene, 2017, 36(38).
在前期的研究中,作者找到了一个新的调控TAM极化的分子,CECR1。该分子的表达与具有促癌作用的M2型巨噬细胞呈相关性,通过诱导M2型极化,能够促进多形性胶质母细胞瘤(GBM)的发生发展。有兴趣的同学可以查阅此篇文献“Activation of CECR1 in M2-like TAMs promotes paracrine stimulation-mediated glial tumor progression”。在今天要讲的文献中,作者上来先通过CECR1与血管新生(CD31)和M2 TAM (CD204) 的相关标志物的表达相关性分析,得出CECR1与CD31,CD204呈现出正相关。
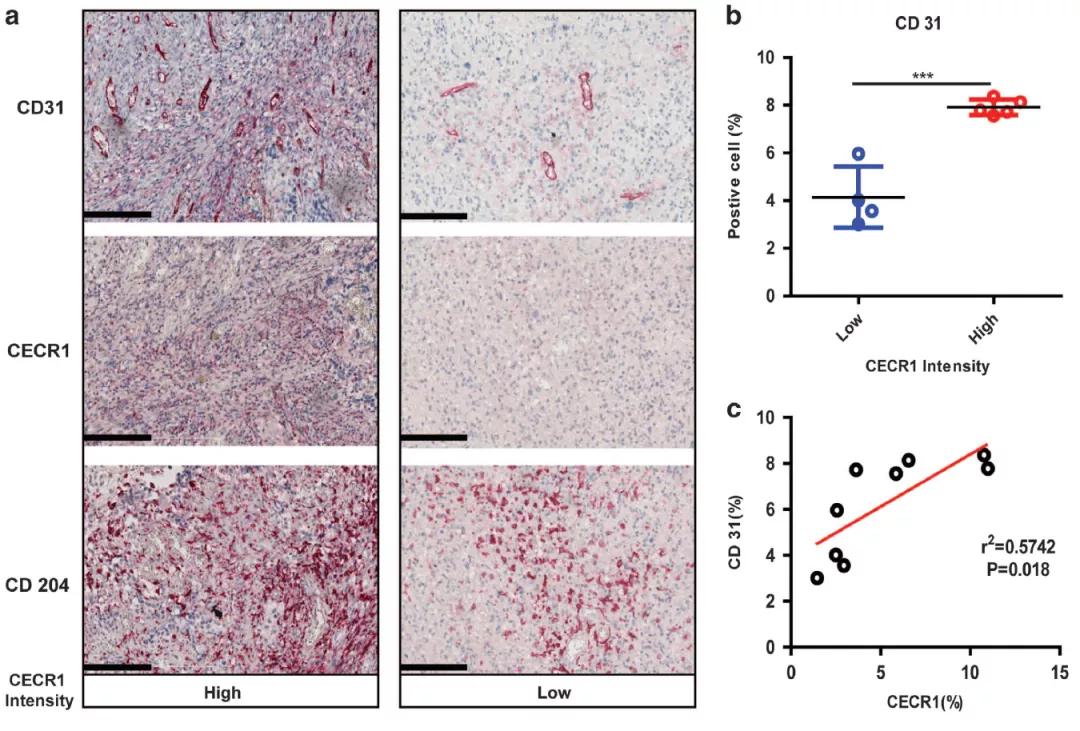
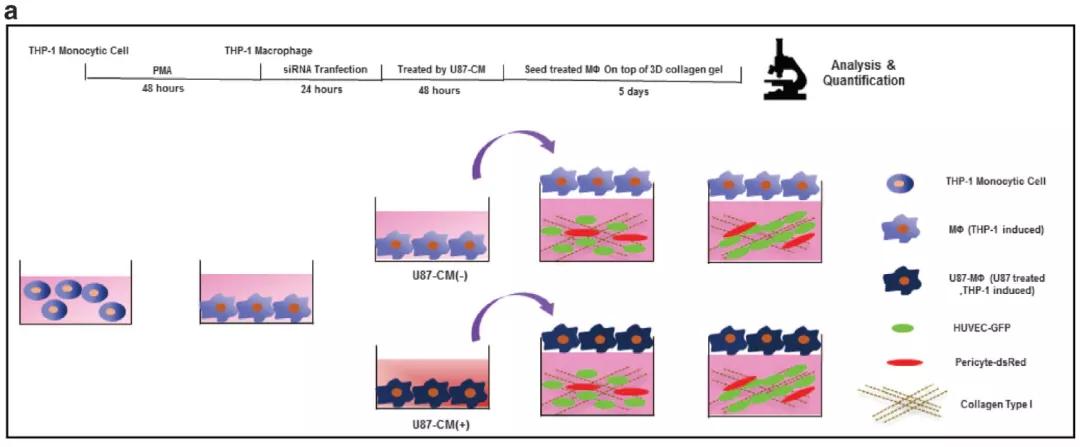
接下来,作者假设CECR1参与了M2型TAM的促血管生成作用。为了验证这一猜想,作者使用了3D共培养技术。通过下面的示意图,我们可以看到,作者使用人单核细胞THP-1细胞系,通过PMA先诱导成Mφ,也就是巨噬细胞。再通过siRNA沉默CECR1。沉默CECR1后使用胶质瘤细胞U87的条件培养基(CM)诱导巨噬细胞成TAM。接下来,作者将不同组的TAM加入在包埋在I型胶原(collagen I)中的周细胞(Pericyte,红色)和血管内皮细胞(HUVEC,绿色)的3D培养体系中。这里需要介绍一下一个新的细胞,周细胞,周细胞是一种包围全身毛细血管和静脉中的内皮细胞的细胞,其可通过物理接触或旁分泌的方式调控血管内皮细胞的功能。
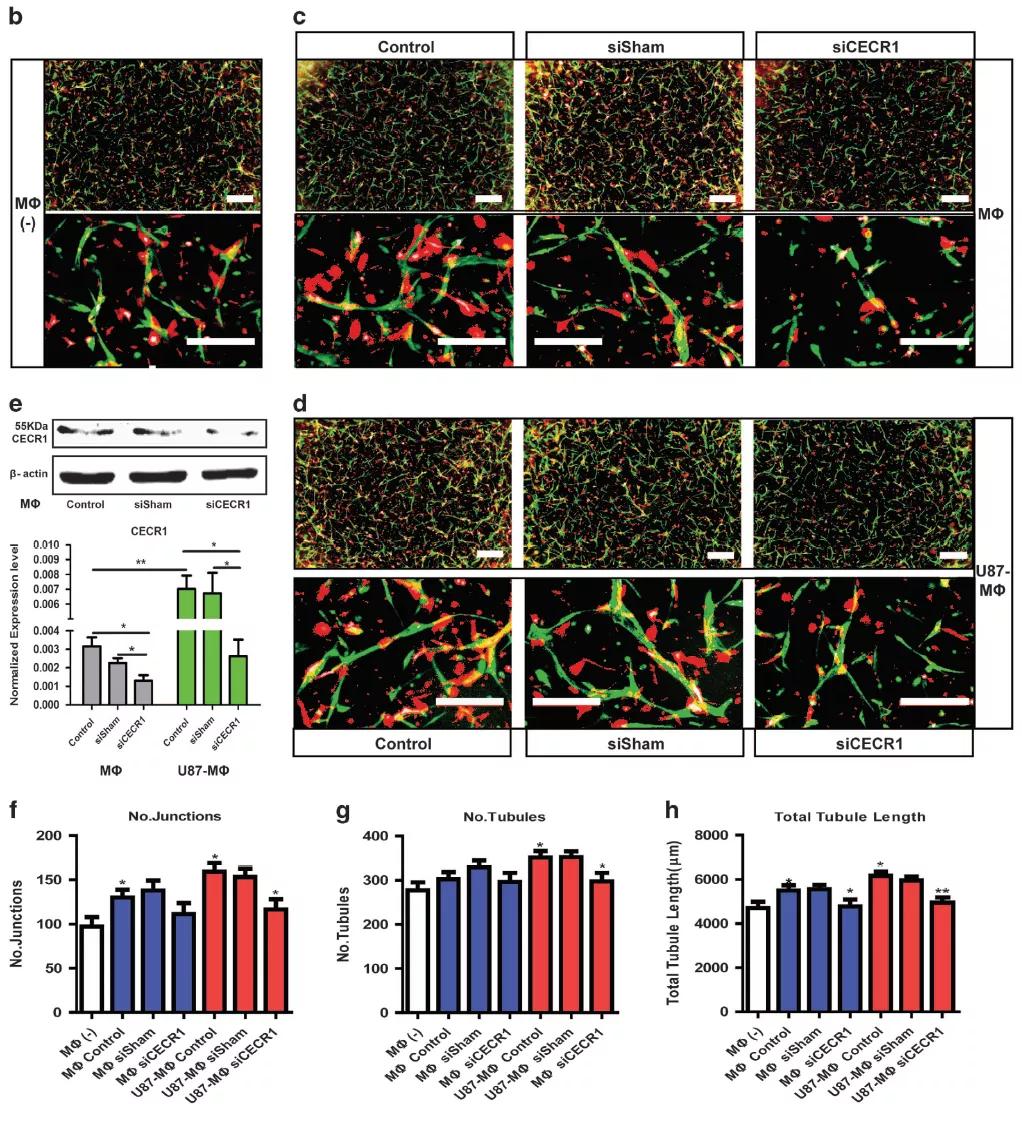
共培养后,作者发现,在共培养体系加入未经CM诱导的Mφ后,能够促进血管形成(图中绿色为GFP标记的HUVEC细胞,红色为dsRed标记的周细胞)。而加入CM诱导的Mφ后,这种促血管生成的作用进一步加强。然而,不管是在诱导还是未诱导的Mφ中沉默CECR1,都能抑制Mφ对血管生成的促进作用。
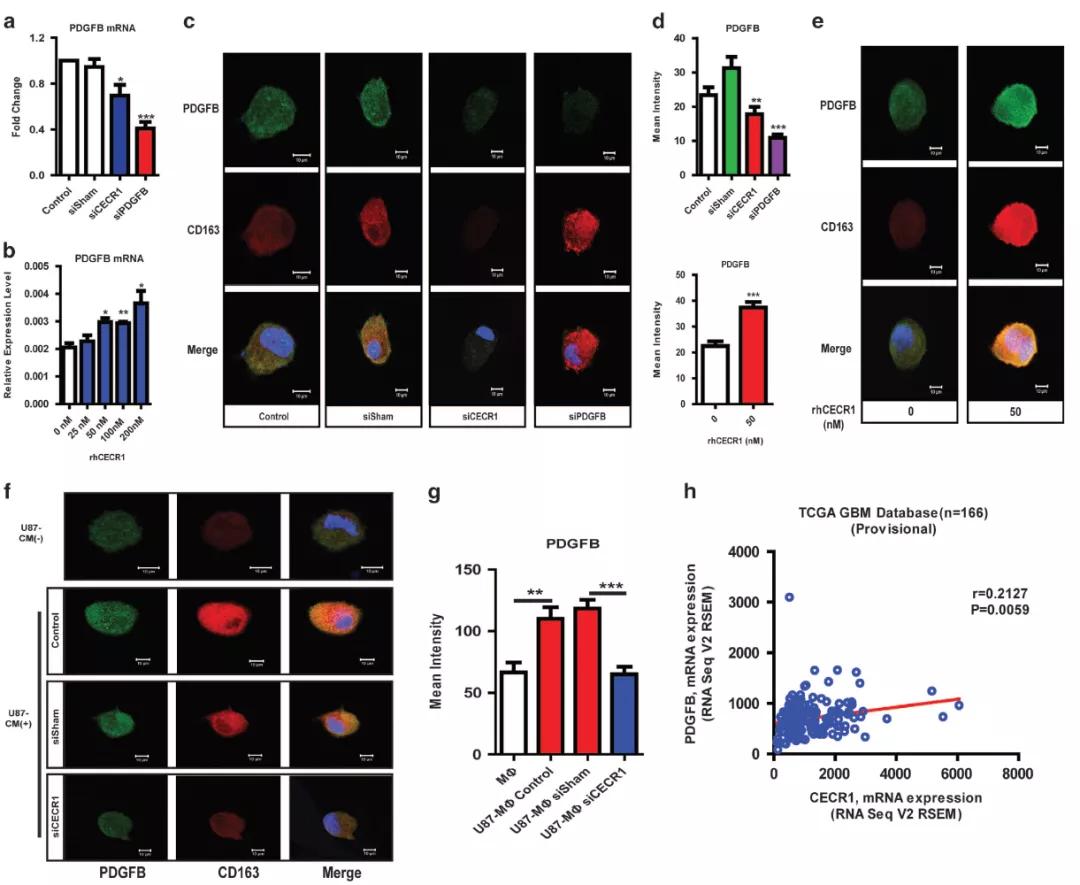
接下来,为了确定哪些已知的促血管生成分子与CECR1的表达相关,作者对9个公认的促血管生成基因(PDGFB、VEGFA、ANGPT1、ANGPT2、MMP7、MMP9、VWF、IL8、Tie-2)进行检测,结果发现沉默CECR1能够显著降低PDGFB的表达(Fig 3a),而过表达 CECR1能够显著增加PDGFB 的表达(Fig 3b), 在fig 3c~3e中,作者通过免疫荧光,进一步证实了qPCR的结果。同时,作者发现U87的CM加入能够诱导巨噬细胞表达PDGFB,而这一作用能够被CECR1沉默所逆转(fig 3f, 3g)。最后,作者还在TCGA数据库中,验证了CECR1与PDGFB呈现正相关性。
作者接下来通过回复实验,证实了在巨噬细胞中沉默PDGFB能够抑制CECR1对巨噬细胞促血管作用的促进作用。结果如下图所示。
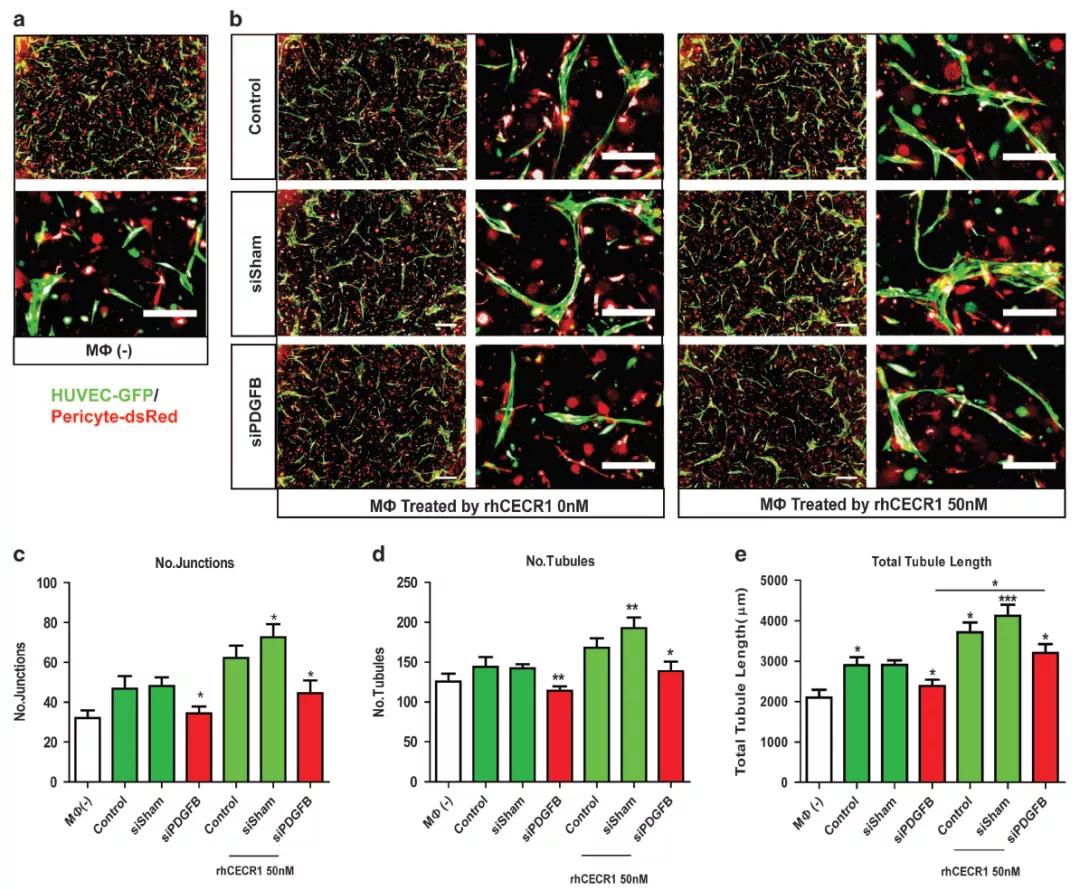
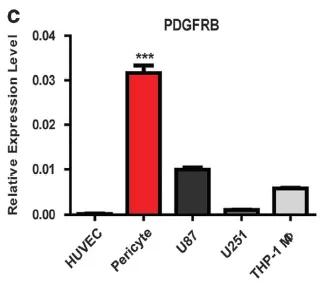
接下来作者通过实验证实, PDGFB的受体PDGFRβ,主要表达在周细胞上。且已知PDGFB/PDGFRβ通路能够促进周细胞的增殖以及周细胞向新生血管的募集和附着以维持新生血管的稳定,那么我们可以跟着作者的思路自然猜测,CECR1介导的巨噬细胞的促血管作用,可能是通过激活周细胞的PDGFB/PDGFRβ通路完成的。
通过将沉默了CECR1,或PDGFB的Mφ的条件培养基诱导周细胞,transwell实验发现CM的加入能够显著诱导周细胞的迁移,而沉默CECR1或PDGFB则无次作用,证实了作者之前的猜测。
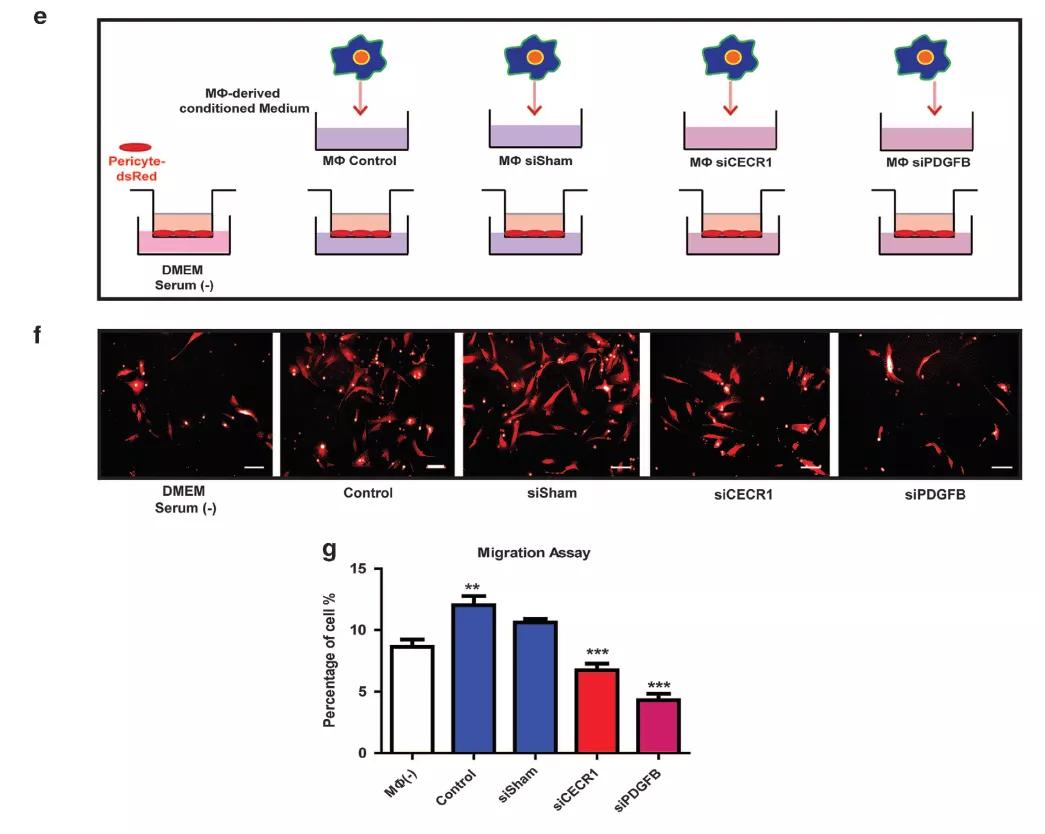
至此,作者基本验证了最开始的猜测,另外再其他结果中作者还发现巨噬细胞的促血管生成作用与促进周细胞分泌Periostin蛋白有关,由于不是文章的主体,在此就不做赘述。总结下来,作者发现了一个新分子CECR1与巨噬细胞的促血管生成作用有关,而这一作用是通过促进巨噬细胞释放PDGFB, 激活周细胞的PDGFB/PDGFRβ通路,产生Periostin蛋白,最终促进血管新生而实现的。这种将我们常见的A分子-B分子-C分子的套路变成A分子-A细胞-B分子-B细胞-C分子-C细胞的方式非常值得我们在课题设计的时候进行借鉴(大家可以思考一下在这篇文献里分别对应的是哪个分子和细胞)。
科研的世界千奇百怪,科研的套路千千万万,以上就是本期推送的内容啦,希望你的脑容量还撑得住。如果有疑问,请给我们留言吧,我们会不定期进行回复的。
