在细胞生物学实验中,Transwell实验绝对是“高频刚需”——不管是研究细胞迁移、侵袭,还是细胞共培养,几乎每个实验室都离不开它。但很多新手(甚至老实验员),常常被“孔径选择、基质胶铺制、结果计数”等问题难住,要么实验重复不出结果,要么数据偏差太大。
把Transwell实验讲透:从核心原理、实验类型,到实操步骤、避坑要点,再到常见问题解答,看完这篇Transwell实验都能从容应对!
先划重点:Transwell实验的核心,是利用“带有微孔的膜”搭建“物理屏障”,模拟体内细胞的迁移/侵袭微环境,核心看“细胞能否穿过屏障”,不同实验类型的差异,本质是“屏障的设置”和“检测目的”不同。
核心提示:Transwell不是“单一实验”,而是“一类实验的统称”,根据检测目的可分为迁移实验、侵袭实验、共培养实验,核心区别在于“是否添加基质胶”和“膜的孔径选择”。
一、Transwell实验核心原理(通俗好懂,一看就会)
用“闯关游戏”类比最直观:Transwell小室就像一个“闯关装置”,小室中间有一张带有微小孔径的聚碳酸酯膜(相当于“关卡屏障”),将培养板分成上下两个腔室。
细胞被接种在“上腔室”,下腔室加入含有趋化因子的培养基(相当于“闯关奖励”),细胞会受到趋化因子的吸引,尝试穿过膜上的微孔,到达下腔室。我们通过计数“成功穿过膜的细胞数量”,来判断细胞的迁移/侵袭能力——穿过的细胞越多,能力越强。
补充关键细节:膜的孔径大小、是否铺基质胶,直接决定实验类型和检测目的;实验的核心是“排除干扰,保证细胞穿过膜的动力仅来自趋化因子”。
二、3种常见Transwell实验类型(重点区分,避免用错)
1. Transwell细胞迁移实验(最基础,无基质胶)
核心目的:检测细胞的“迁移能力”——即细胞在无基质阻挡的情况下,向趋化因子方向移动的能力,模拟体内细胞的“自由迁移”过程(如炎症细胞向病灶迁移)。
关键操作:不铺基质胶,直接将细胞接种在上腔室,下腔室加入趋化因子(如血清、细胞因子),培养一定时间后,固定、染色,计数穿过膜的细胞。
膜孔径选择:根据细胞大小选择,常用8μm(适合肿瘤细胞、成纤维细胞等);如果是白细胞等小型细胞,可选择5μm。
应用场景:肿瘤细胞迁移能力检测、药物对细胞迁移的影响、细胞迁移相关基因的功能验证。
2. Transwell细胞侵袭实验(进阶,铺基质胶)
核心目的:检测细胞的“侵袭能力”——即细胞穿过“基底膜样基质”的能力,模拟体内细胞突破组织屏障的过程(如肿瘤细胞侵袭周围组织、转移)。
关键操作:在上腔室的膜表面,铺一层Matrigel基质胶(模拟体内基底膜),基质胶凝固后接种细胞,下腔室加入趋化因子,细胞需要先降解基质胶,再穿过膜,才能到达下腔室。
核心区别:比迁移实验多了“基质胶降解”的步骤,更贴近体内肿瘤侵袭的真实场景,能同时检测细胞的“迁移能力”和“基质降解能力”。
应用场景:肿瘤侵袭能力检测、转移相关基因/蛋白的功能验证、抗肿瘤药物的侵袭抑制效果评估。
3. Transwell细胞共培养实验(特殊用途,无/有基质胶均可)
核心目的:实现“两种细胞的间接共培养”,研究细胞间的旁分泌作用(即一种细胞分泌的因子,影响另一种细胞的功能),无需直接接触,避免细胞间直接作用的干扰。
关键操作:上腔室接种一种细胞(如肿瘤细胞),下腔室接种另一种细胞(如基质细胞),膜的孔径选择3μm或0.4μm(阻止细胞穿过,仅允许细胞分泌的因子通过),培养一定时间后,检测两种细胞的功能变化(如增殖、分化、蛋白表达)。
灵活调整:若需要研究细胞间的“直接接触共培养”,可去除膜,或使用可通透的膜(0.4μm),根据实验需求调整。
应用场景:肿瘤微环境研究(如肿瘤细胞与成纤维细胞的相互作用)、干细胞分化调控、细胞间信号传导机制研究。
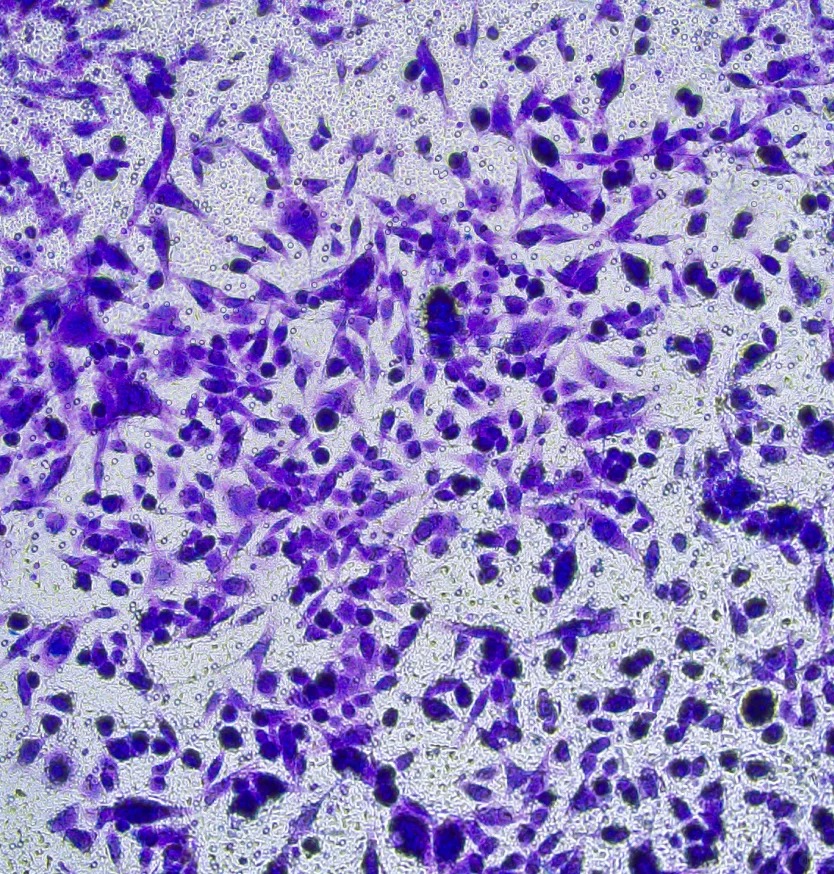
- Q:迁移实验和侵袭实验,除了基质胶,还有其他区别吗?A:核心区别是“是否需要降解基质”,迁移实验无需降解,仅检测细胞移动能力;侵袭实验需要细胞分泌基质金属蛋白酶(MMPs)降解基质胶,更贴近体内侵袭场景。
- Q:细胞穿过膜后,怎么确保计数准确?A:随机选取5个不同视野(避开边缘),用显微镜计数,计算平均值;若细胞数量过多,可稀释染色后计数,避免漏数或重复计数。
- Q:共培养实验,膜的孔径怎么选?A:仅研究旁分泌作用,选3μm或0.4μm(阻止细胞穿过,允许因子通过);需要细胞直接接触,选8μm或10μm(允许细胞穿过,实现直接共培养)。