🔥 什么是GST-pulldown技术?原理简单,精准能打!
2. 亲和捕获:将纯化后的GST-诱饵蛋白,与谷胱甘肽琼脂糖树脂孵育,GST标签会与树脂上的谷胱甘肽特异性结合,使诱饵蛋白固定在树脂上,形成“诱饵蛋白-树脂复合物”,特异性排除非靶标蛋白干扰
不同于其他蛋白互作检测技术,GST-pulldown技术可在体外模拟细胞内蛋白互作环境,既能验证已知蛋白间的互作关系,也能筛选未知的互作蛋白,且操作流程标准化,重复性强,是蛋白互作研究的首选技术。
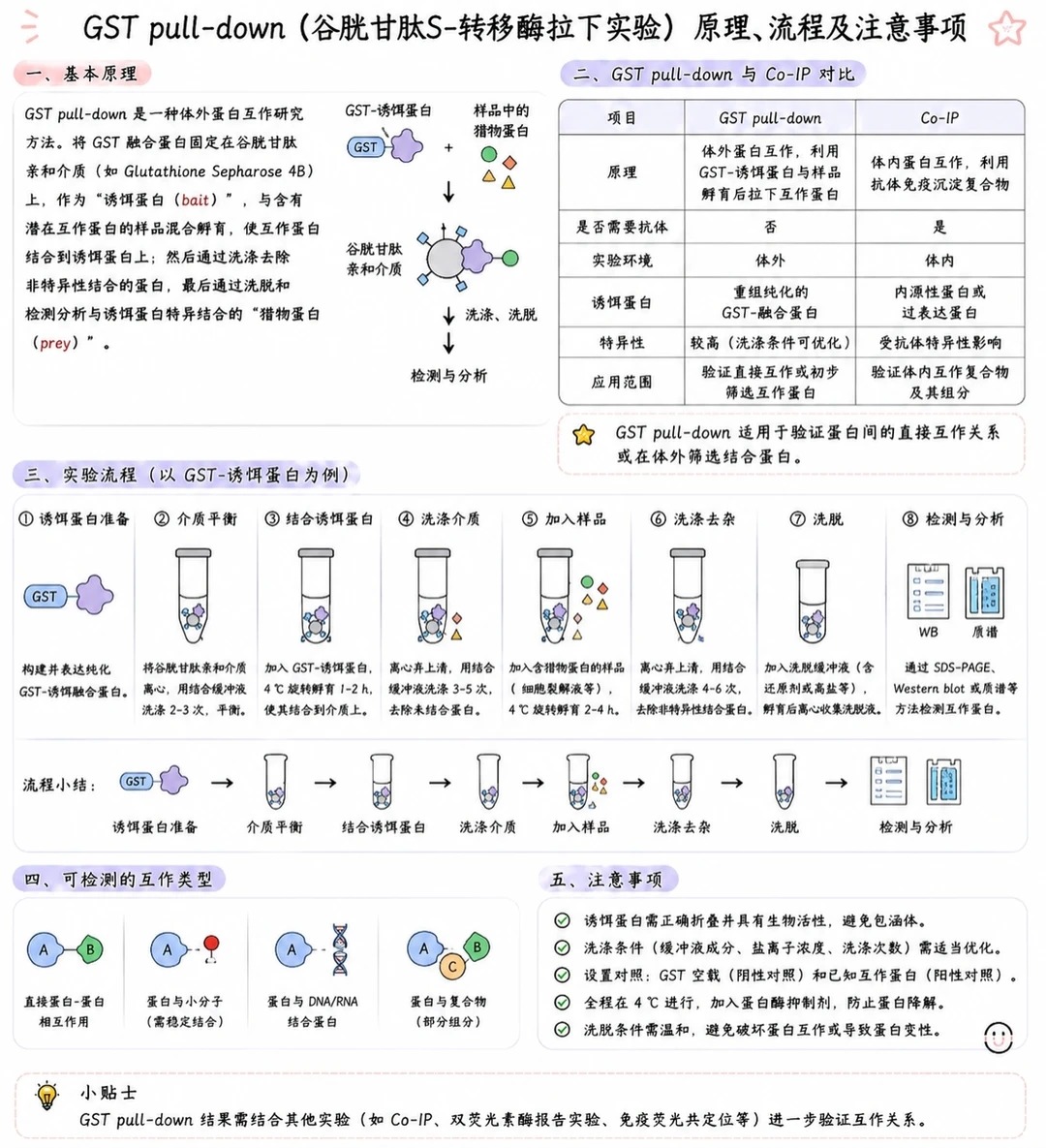
📌 研究蛋白-蛋白相互作用的常用体外方法之一:GST pull-down 它的核心思路其实很直观👇 👉 将 GST融合蛋白 作为“诱饵蛋白(bait)”固定在谷胱甘肽亲和介质上 👉 再加入含候选互作蛋白的样品孵育 👉 如果两者能够结合,目标蛋白就会被“拉下”并富集下来 👉 最后通过洗涤去除非特异结合蛋白,再进行检测分析 和 Co-IP 相比,GST pull-down 更偏向体外直接结合验证,常用于证明蛋白之间是否存在直接互作,也可作为筛选候选结合蛋白的方法之一。 基本流程:构建并表达GST融合蛋白 → 与谷胱甘肽介质结合 → 加入样品孵育 → 洗涤去除非特异结合 → 洗脱 → 检测与分析。 看起来流程清晰,但细节很关键⚠️ ✔ GST融合蛋白要保证正确折叠并具有活性 ✔ 全程尽量低温操作,通常在 4°C 进行 ✔ 洗涤条件要合适,避免背景过高或信号过弱 ✔ 一定要设置 GST空载对照 和已知互作对照 💡一句话总结: GST pull-down看的是“能不能在体外直接拉下来”,关键在诱饵蛋白、洗涤条件和对照设计。