做蛋白原核表达你是否也遇到这些问题![]()
目的蛋白不表达或表达量低?目的蛋白形成包涵体?目的蛋白降解?蛋白纯化困难?别着急!完全可以解决!
1、目的蛋白不表达或表达量低
1. 优化目的基因序列:通过生物信息学软件分析目的基因序列,将稀有密码子替换为宿主菌(如大肠杆菌)偏好的同义密码子,同时优化mRNA二级结构,提升翻译效率
2. 匹配表达载体与宿主菌:根据目的蛋白特性选择合适的表达载体,如需要高表达可选择T7启动子载体,需要调控表达可选择lac启动子载体;若目的蛋白对宿主菌有毒性,选用BL21(DE3)pLysS菌株,其含有的溶菌酶基因可降低本底表达,减少毒性影响;若目的蛋白存在二硫键错配问题,可选用OrigamiB(DE3)、Shuffle T7等菌株,辅助二硫键正确折叠。
3. 优化诱导条件:诱导剂(如IPTG)浓度优化为0.1~1.0 mmol/L;诱导时机选择宿主菌生长至对数中期(OD600=0.6~0.8);诱导温度根据蛋白特性调整,提升表达量;部分蛋白可采用分步诱导策略,初期低浓度诱导剂启动表达,逐步增加浓度,控制翻译速率。
4. 改善目的蛋白表达特性:若目的蛋白疏水性强、分子量过大,可采用融合表达策略,将目的蛋白与可溶性标签(如GST、MBP、SUMO)融合,改善蛋白溶解性和表达量,后续可通过酶切去除标签;若目的蛋白对宿主菌有毒性,可采用低温诱导、低浓度诱导,或构建诱导型表达载体,减少对宿主菌的损伤;对于小分子量(<10 kDa)易降解的蛋白,可通过融合标签增加其稳定性,避免降解导致的表达量降低。
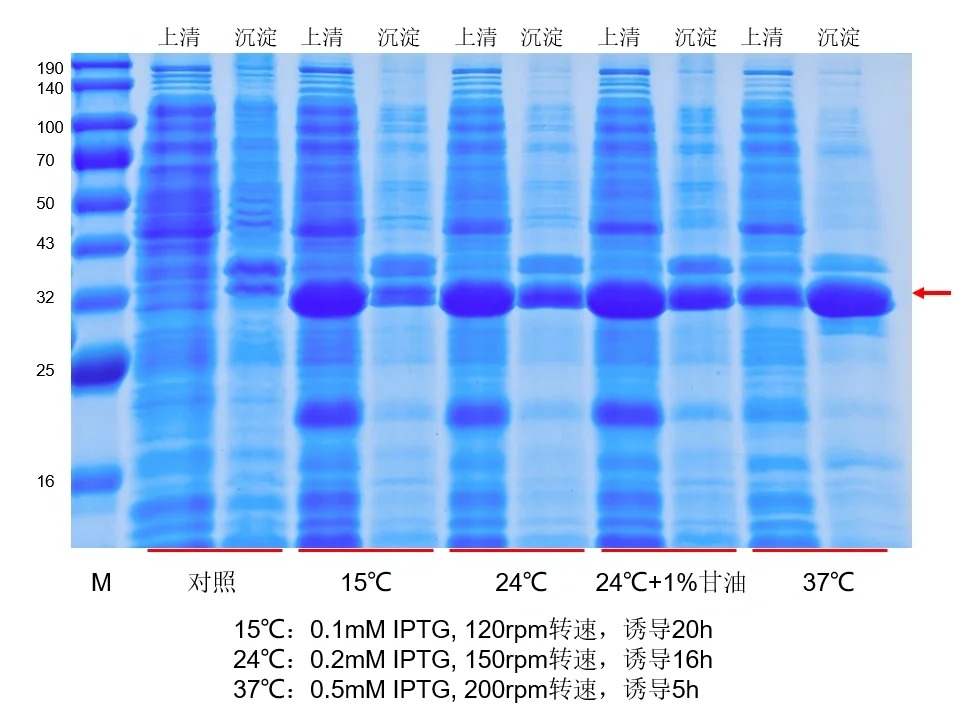
2、目的蛋白形成包涵体
包涵体是外源基因在原核宿主菌中高效表达时,形成的高密度、不溶性蛋白质颗粒,主要成分为密集堆积的变性蛋白分子,在光学显微镜下可见,直径约0.5~0.8 μm,其形成的核心原因是目的蛋白在宿主菌内快速大量表达,折叠速度滞后于合成速度,导致疏水基团暴露,蛋白分子之间发生聚集,最终形成不溶性沉淀。
1. 预防包涵体形成:优化诱导条件,降低诱导温度(16~25℃)、减少诱导剂浓度(0.1~0.5 mmol/L)、延长诱导时间,减缓蛋白合成速度,给予新生肽链充足的折叠时间;共表达分子伴侣,将目的基因与GroEL/GroES、DnaK/DnaJ等分子伴侣基因共克隆至表达载体,共转化宿主菌,辅助目的蛋白正确折叠,减少聚集;优化培养基成分,添加甘氨酸、脯氨酸等有助于蛋白折叠的氨基酸,或添加甘油、山梨醇等渗透压保护剂,维持宿主菌内环境稳定,促进蛋白折叠;调整培养基pH值至7.0~7.5,维持中性或略偏碱性环境,有利于大多数蛋白的正确折叠;采用融合表达,将目的蛋白与可溶性标签融合,改善蛋白疏水性,减少聚集。
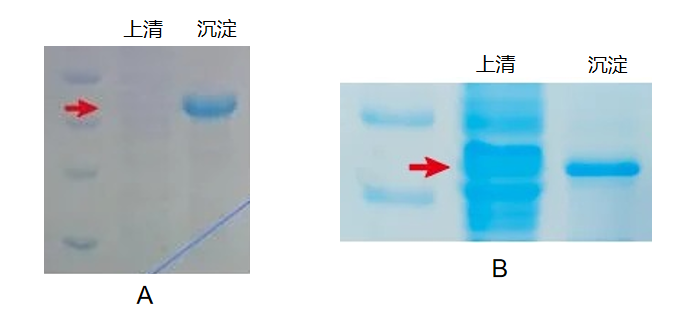
2. 包涵体的溶解与复性:若包涵体已形成,可通过溶解-复性过程获取具有生物活性的可溶性蛋白。复性过程中需严格控制温度、pH值和复性速度,避免蛋白再次聚集,提升复性效率——目前包涵体复性效率较低,仍是原核表达中亟待优化的环节,不同蛋白的复性方法需通过实验逐步筛选。蛋白纯化史:A-B(从包涵体到可溶性蛋白)
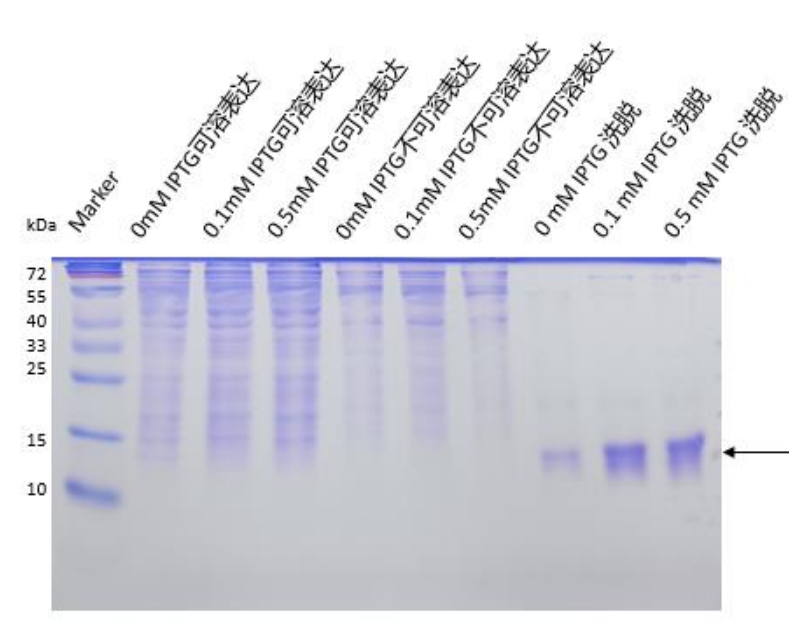
3、目的蛋白降解
1. 抑制蛋白酶活性:选用蛋白酶缺陷型宿主菌,如BL21(DE3)、BL21(DE3)pLysS等,其缺失主要的蛋白酶基因,可显著减少目的蛋白降解;在培养基、破碎缓冲液、纯化缓冲液中添加蛋白酶抑制剂(如PMSF、EDTA、抑肽酶),其中PMSF需现配现用,避免失效;破碎宿主菌时采用低温操作(4℃或冰浴),降低蛋白酶活性,减少蛋白降解。
2. 优化诱导与培养条件:缩短诱导时间,根据蛋白表达规律,在目的蛋白表达量达到峰值时终止诱导,避免蛋白长时间停留于宿主菌内;控制培养温度,采用低温诱导(16~25℃),不仅可减少包涵体形成,还可降低蛋白酶活性;优化培养基成分,添加葡萄糖等碳源,抑制宿主菌蛋白酶的表达和活性。
3. 增强目的蛋白稳定性:采用融合表达,将目的蛋白与GST、MBP等标签融合,增加蛋白分子量和稳定性,减少降解;对目的蛋白进行定点突变,修饰蛋白酶识别位点,降低被降解的概率;纯化后的蛋白及时透析、浓缩,添加甘油(终浓度20%~50%),-80℃保存,避免反复冻融,减少降解。
4. 优化纯化操作:纯化过程全程低温,避免剧烈搅拌和反复离心;选用合适的纯化方法,尽快完成纯化流程,缩短蛋白暴露于蛋白酶的时间;若出现截短蛋白,可选用两端带有融合标签的载体(如pET-28、pET-30系列),通过提高洗脱剂浓度,将截短蛋白与全长蛋白分离,获得完整目的蛋白。
4、蛋白纯化困难
1. 优化纯化前处理:若目的蛋白为包涵体,需彻底洗涤包涵体,去除杂蛋白和脂类杂质,避免杂蛋白干扰纯化;若目的蛋白为可溶性蛋白,破碎宿主菌后离心去除沉淀,上清液经0.22 μm滤膜过滤,去除微小杂质和核酸复合物,提升纯化效率;可在纯化前添加核酸酶,降解宿主菌核酸,减少核酸与目的蛋白的结合,降低纯化难度。
2. 优化亲和纯化条件:若亲和标签被掩盖,可通过优化缓冲液pH值、离子强度,或添加温和变性剂(如低浓度尿素),暴露标签位点,促进与亲和介质结合;调整洗脱条件,采用梯度洗脱法,根据目的蛋白与标签的结合强度,逐步提高洗脱剂浓度,减少杂蛋白洗脱,提升纯化纯度;若His标签纯化效果不佳,可更换标签(如GST、MBP),或采用双标签融合表达,提高纯化特异性。
3. 组合纯化策略:单一纯化方法难以获得高纯度蛋白,可采用“亲和纯化+凝胶过滤层析+离子交换层析”的组合策略,先通过亲和纯化快速富集目的蛋白,再通过凝胶过滤层析去除聚合体和大分子杂蛋白,最后通过离子交换层析去除小分子杂蛋白,逐步提升蛋白纯度;对于复性后的蛋白,可通过凝胶过滤层析去除未复性的蛋白和变性剂,获得具有生物活性的高纯度目的蛋白。
4. 避免纯化过程中蛋白变性:全程低温操作(4℃或冰浴),缓冲液中添加蛋白酶抑制剂和抗氧化剂(如DTT、β-巯基乙醇),防止蛋白降解和氧化;避免剧烈搅拌、反复冻融和过高离心速度,减少蛋白构象变化;根据目的蛋白特性选择合适的缓冲液体系,维持蛋白天然构象,避免变性。
![]() 我们拥有一支深耕蛋白原核表达领域多年的技术团队,具备丰富的实验实操经验和问题解决能力,可根据您的目的蛋白特性、实验需求,定制专属的表达与纯化优化方案,协助您快速攻克实验痛点,提升实验效率、降低实验成本。无论是基础实验的技术指导、疑难问题的在线答疑,还是定制化实验服务的落地执行,我们都将全程保驾护航,助力您的科研与生产工作高效推进。
我们拥有一支深耕蛋白原核表达领域多年的技术团队,具备丰富的实验实操经验和问题解决能力,可根据您的目的蛋白特性、实验需求,定制专属的表达与纯化优化方案,协助您快速攻克实验痛点,提升实验效率、降低实验成本。无论是基础实验的技术指导、疑难问题的在线答疑,还是定制化实验服务的落地执行,我们都将全程保驾护航,助力您的科研与生产工作高效推进。
如需获取更精准的技术支持、咨询定制化服务,或索要实验优化相关资料,欢迎随时联系我们:18570028002 或 微信 pulateze666
我们始终以专业、高效、贴心的服务,助力每一位科研与生产工作者,突破蛋白原核表达实验瓶颈,解锁实验新可能!