
随着医学生物领域研究的日新月异,除了坏死以外,科学家们陆续发现了其他细胞死亡形式,大致可分为程序性细胞死亡包括细胞凋亡、细胞焦亡和自噬,以及非程序性细胞死亡包括副凋亡、细胞有丝分裂灾难和胀亡等。2012年,Dixon等正式提出并命名了一种区别于细胞凋亡、细胞焦亡、细胞自噬的新的细胞死亡形式:铁死亡!
01
铁死亡相关特征
生物学特征:活性氧、铁离子聚集,激活丝裂原活化蛋白激酶(MAPK)系统,胱氨酸摄取减少、谷胱甘肽耗竭,抑制systemXc-;
基因水平:主要受到核糖体L8(RPL8)、铁反应元件结合蛋白(IREB2),ATP合成酶F0复合体亚基C3(ATP5G3)、三四肽重复结构域35(TTC35)、柠檬酸合成酶(CS)、酰基辅酶A合成酶家族成员2(ACSF2)以及受代谢、储存基因TFRC、ISCU、FTH1、FTL、SLC11A2的调节。
02
铁死亡部分机制
抑制胱氨酸谷氨酸转运受体 (systemXC-)诱导铁死亡:通过systemXC-,谷氨酸与胱氨酸以1:1比例交换,因此,谷氨酸的水平会影响到systemXC- 的功能。细胞外高浓度的谷氨酸会抑制systemXC-从而诱导铁死亡。敲除systemXC-的小鼠由于细胞外谷氨酸水平减少,可以防止神经毒性损伤。
p53介导铁死亡:p53是一种抑癌基因,通过下调systemXC-组分SLC7A11的表达抑制细胞对胱氨酸的摄取,导致谷胱甘肽过氧化物酶活性降低,削减细胞抗氧化能力,增强细胞对铁死亡的敏感性。同时,研究发现,在人肿瘤细胞中SLC7A11过度表达,这种过表达能够抑制活性氧诱导的“铁死亡”,同时削弱p53 3KR介导的对肿瘤生长的抑制作用。
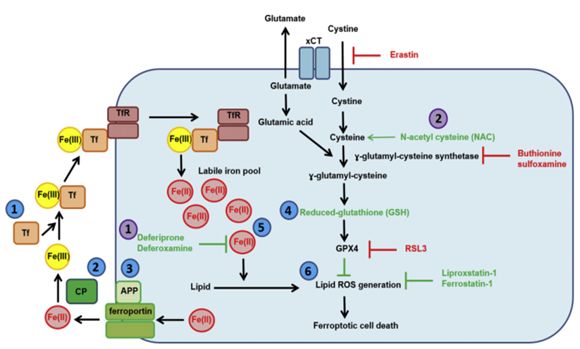
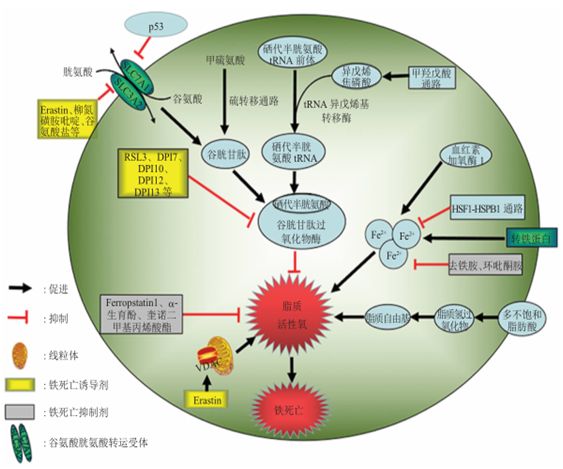 铁死亡机制
铁死亡机制
03
检测指标
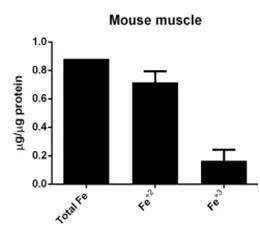
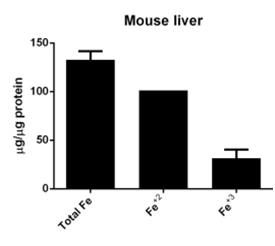
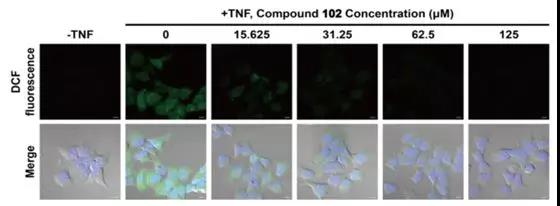
qRT-PCR/WB检测:检测与铁死亡相关的蛋白表达,如PTGS2、NOX1、FTH1、COX2、GPX4、ACSL4等,其中COX2、ACSL4、PTGS2、NOX1在铁死亡细胞中表达上调,GPX4、FTH1在铁死亡细胞中表达下调;
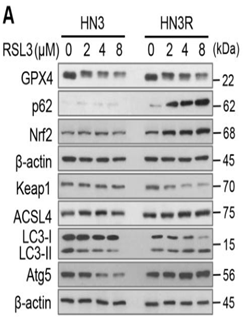
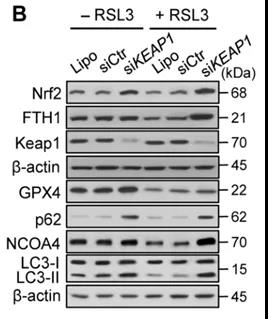
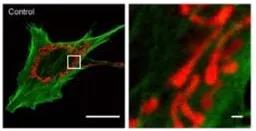
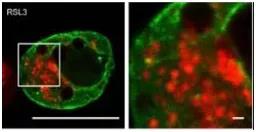
透射电镜直接观察细胞形态;
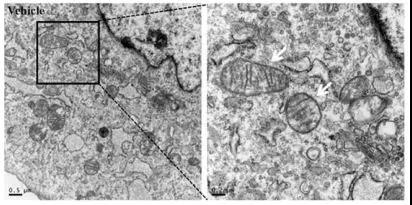
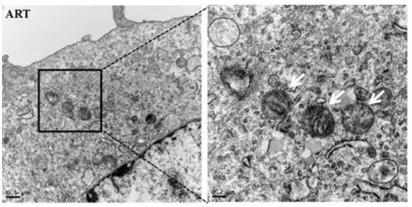
线粒体观察:向细胞内转染LifeAct-GFP荧光蛋白,一段时间后用有丝分裂追踪器观察线粒体形态。
04
铁死亡与疾病的关系
4.1 铁死亡与肿瘤
最近研究证明,铁死亡很有可能是引起PD神经退行性变细胞死亡的通路之一,铁是治疗PD的有效靶点。在细胞和MPTP诱导的PD小鼠模型中运用铁螯合剂(去铁酮),能减少氧化应激,增强多巴胺可利用性,从而改善现有的运动症状和减少运动功能的退化。早期阶段的PD患者中,应用去铁酮治疗可减缓运动缺陷的进展,减少现有的运动症状。在MPTP治疗前24小时给小鼠注射铁死亡抑制剂ferrostatin-1可显著挽救行为障碍和神经元丢失,这表明常见的PD毒素在动物模型中引起神经退行性变的机制可能是铁死亡。
05
结语
End
更多细胞铁死亡相关知识,尽在春风学院:http://weike.fm/O1JVz187af,点此跳转
凭优惠码616联系客服,即可获得本视频优惠券~课程为付费视频,禁止转发





